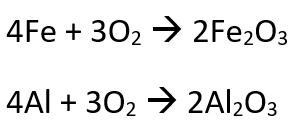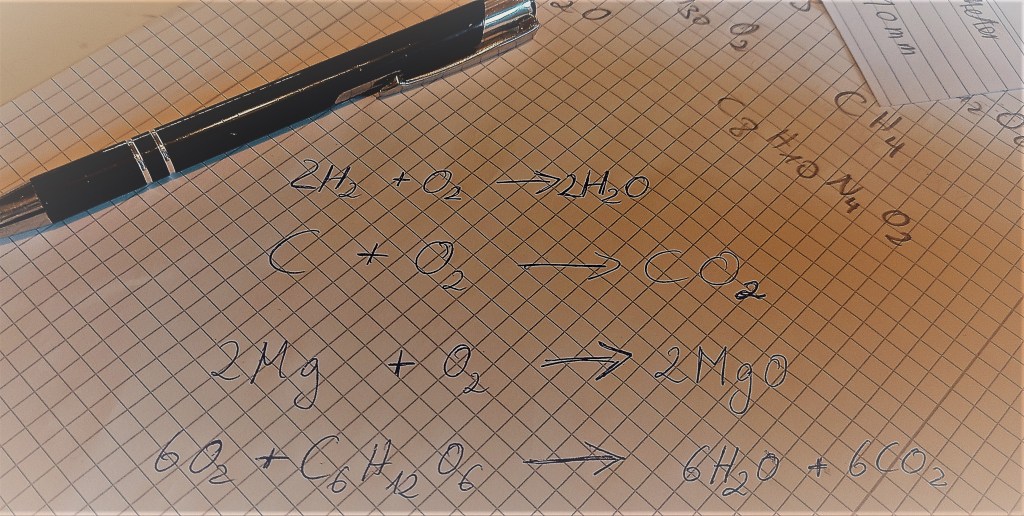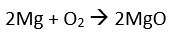Für viele von euch sind die Schulferien schon vorbei. So auch für mich und meine Kinder. Dieses Jahr ging es erneut ans Meer. Wie viele andere, die die Möglichkeit dazu haben, in den Sommerferien wegzufahren. Dabei folge ich der Mehrheit. Laut einer Statistik von Statista und TNS Emid aus dem Jahr 2015 fahren 70% der Deutschen lieber ans Meer, 23% in die Berge und 7% wissen es nicht oder machen keine Angaben. Aber warum Urlaub? Das ist sicher sehr individuell.
Ich möchte im Urlaub mal runterkommen. Dem Alltag mit Arbeit, Chemie-Edutainment und gewohntem Haushalt entfliehen. Den Kopf frei kriegen. Und frage mich dabei: Kann ich der Chemie wirklich entfliehen?
Am Strand stecke ich meine Füße in warmen Sand und schaue auf das blaue, Gischt geschäumte Wasser. Sand… SiO2… Glas… Kristallstruktur… Da sind die Gedanken wieder und ich lasse sie treiben wie den Drachen an der Schnur. Kommt doch mit auf meine kleine chemische Reise durch meinen Urlaub am Meer…

Am ersten Tag geht es schon an den Strand. Es ist so ein schönes Gefühl, die Füße in den warmen, weichen Sand zu stecken. Kleine Muscheln und Steinchen zu spüren, das Rieseln kitzelt. Und Gedanken kommen. Sand ist eine Mischung, er besteht aus unterschiedlichen Mineralien. Er besteht aus Quarz SiO2, Calciumcarbonat CaCO3, Olivin und Basalt – das sind Silikate X(SiO4), Magnetit – eine Eisenverbindung Fe3O4, und Gips Ca(SiO4)x2H2O. Je nachdem, an welchem Strand ihr eure Füße in den Sand steckt. Ganz schön chemisch.
Zurück am kleinen Bungalow in der Ferienanlage im Süden Frankreichs muss ich erst einmal etwas trinken. Es ist heiß und ich fühle mich von Sonne, Sand und Meer ausgetrocknet. Schnell ein Glas Wasser, oder besser zwei. Moment… Glas? Viele wissen, dass Glas aus Sand hergestellt wird. Die Glasherstellung ist eine Technologie, die sehr stark mit der Entwicklung der Menschheit und der Gesellschaft einher geht. Glas wird seit vielen Tausend Jahren hergestellt. Das älteste, datierbare Glasgefäß, das heute noch erhalten ist, stammt aus Altägypten aus dem Jahr 1450 v. Chr. Ist also 3.475 Jahre alt. Der Kelch steht jetzt in einem Museum. Heutzutage stellt man Glas nicht einfach aus Sand her. Denn Sand ist eine Mischung unterschiedlichster Mineralien. Glas wird aus reinem Quarz SiO2, einer Verbindung aus Silizium und Sauerstoff hergestellt. Um Farbe und Eigenschaften des Glases zu ändern, werden noch bestimmte Stoffe beigemischt.

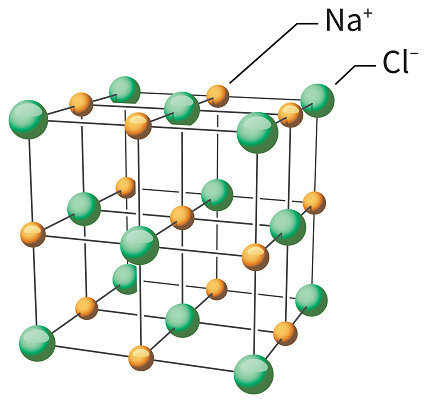
Jetzt bin ich erst mal wieder gut hydriert und ich kann auch etwas klarer denken. Auf der Liege grübel ich weiter über Glas. Wie sieht es da drin eigentlich aus? Was könnte entdeckt werden, wenn mit einem riesig großen, starken Mikroskop immer näher in das Glas hineingezoomt werden könnte? In dem chemischen Stoff SiO2 kommen auf ein Siliziumatom genau zwei Sauerstoffatome. Das ist immer so. Man spricht auch von dem Gesetz der konstanten Proportionen, dieses gilt nicht nur für SiO2 sondern ist ein Grundprinzip der Chemie: Eine bestimmte chemische Verbindung setzt sich immer aus den gleichen Atomen in gleicher Verknüpfung und Anzahl zusammen. Würde sich das ändern, wäre es ein anderer chemischer Stoff. Hineingezoomt in Glas würde man also immer abwechselnd und regelmäßig Atome entdecken: Bei Quarz SiO2 sind die Atome in einem regelmäßigen Kristallgitter zusammengesetzt, man spricht auch von einer Salz-Verbindung. Jede Atomsorte hat einen festen Platz, und dieser wiederholt sich regelmäßig, bis das Ende des Kristalls erreicht ist. Und das dauert. Denn es sind richtig viele Atome in einem Kristall enthalten. In einem Kilo Sand stecken 10.000.000.000.000.000.000.000.000 Einheiten SiO2 – das sind 10 Quadrillionen. Ganz schön viel Chemie im Sand. Wie viel das wohl am gesamten Strand wäre?
Das war viel. Und ich muss erstmal den Kopf wieder klar kriegen. Ich lege den Kopf nach hinten und schaue hoch. Sehe den blauen Himmel, höre die Zikaden rufen. Weiße Wolken ziehen, die Kronen der Kiefern bewegen sich langsam. Herrlich zu entspannen. Als ich so nach oben in die Wipfel der Kiefernbäume schaue und den aromatischen, harzigen Duft einatme, denke ich an Zellulose in den Kiefernnadeln und an komplexe Mischungen aus Terpenoiden, Harzsäuren, Polymere und ätherischen Öle. Ich denke an den Kunststoff Polyvinylchlorid PVC, aus dem der Wasserball meiner Tochter besteht und den Weichmacher Di-isononylphthalate, der da drin steckt und den Wasserball so elastisch macht. Langsam werde ich müde. Es wird warm, ich mache die Augen zu und schlafe langsam ein. Es war ein langer Tag.

Ein Gewitter weckt mich. Unbemerkt hat sich der Himmel verdunkelt und die Schwüle entlädt sich mit Blitzen und Donnern. Schlagartig wird mir bewusst, wie wichtig Elektronen für die Chemie ist: Bei der Bildung von SiO2 (Quarz / Sand) gehen zwei Elektronen vom Silizium auf den Sauerstoff über. Es entsteht eine Ionenbindung, aus Salz-Verbindung genannt. Und was hat das mit dem Gewitter zu tun? Blitze sind Ausgleich von elektrischer Ladung durch Elektronen. Blitze können so heiß werden, dass beim Einschlag aus Sand durch Schmelzprozesse auch Glas entstehen kann. Und Blitze spielen laut der Abiogenese Theorie eine wichtige Rolle bei der Entstehung des Lebens aus unbelebter Chemie. Chemische Evolution wird das genannt. Chemie und Physik haben schöpferische Kräfte. Und mit dem Gedanken schlafe ich wieder ein.
Am nächsten Tag gehe ich erneut ans Meer. Der Anblick des Meeres ist so überwältigend und beruhigend für mich. Damit fühle ich mich sicher nicht allein. In meinem Kopf geht es jedoch noch etwas chemischer zu: Neben den Ionenbindungen im Sand und im Salz gibt es kovalente Bindungen, auch Molekülbindungen genannt. Ein klassisches Beispiel dafür ist Wasser H2O.

In einem Wassermolekül, das aus einem Sauerstoffatom und zwei Wasserstoffatomen besteht, teilen sich je ein Wasserstoffatom und ein Sauerstoffatom einige Elektronen und erzeugen dadurch eine Bindung. Ich schmunzel ein bisschen und muss bei dem Wort Bindung auch an Zwischenmenschliches Denken. Wer weiß, gibt es da Parallelen? Manchmal entsteht Bindung durch Anziehung von Gegensätzlichem, manchmal durch Gemeinsamkeiten. Auf alle Fälle spielt Energie eine große Rolle dabei.
Eine dritte Bindungsart ist übrigens die Metallbindung. Das geht mir beim nachmittäglichen Boule-Spiel durch den Kopf. Boule ist in meiner Empfindung ein Nationalsport in Frankreich, insbesondere in der Variante Pétanque, welches in der Gegend Südwest Frankreich mit Metallkugeln gespielt wird. Und bei Metall denke ich an Chemie und an Elektronen. In einem Metall schwirren Elektronen losgelöst als Elektronengas um positiv geladene Atomrümpfe. Jetzt direkt mal richtig laut Metal-Musik anmachen und ordentlich den Kopf schütteln. Das passt richtig gut zu meiner Vorstellung, was in einem Metall bindungsmäßig abgeht. Ganz schön viel. An welche Musik denkt ihr bei Metall?

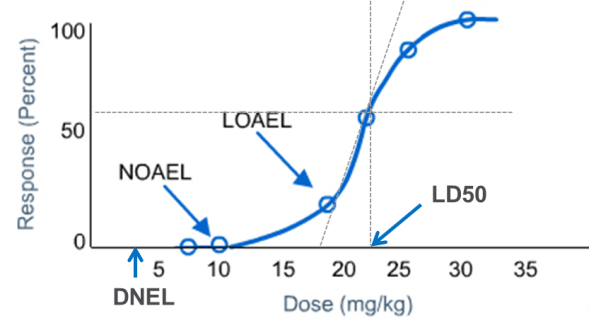
Ich habe übrigens richtig Spaß an dem Spiel und traue mich sogar, an einem kleinen Turnier teilzunehmen. Vor vielen Jahren habe ich als Jugendlicher auch schon mit Franzosen Boule gespielt. Und damals kein einziges Spiel gewonnen. Es gab immerhin als Trostpreis eine Flasche Rosé für mich. In diesem Urlaub sitze ich nach dem Ausscheiden im Achtelfinale mit einer Flasche alkoholfreiem Bier am Platz und schaue den Franzosen beim weiteren Tournier zu. Was ist eigentlich Alkohol? Alkohol ist eine typische organische Verbindung. Organische Verbindungen enthalten im Gegensatz zu anorganischen Verbindungen (Salz oder Sand) immer Kohlenstoff und Wasserstoff. Alkohol, auch Ethanol genannt hat die Strukturformel CH3CH2OH. Neben den tollen und wichtigen Eigenschaften als Lösemittel und Desinfektionsmittel ist Alkohol lebertoxisch und krebserregend. Interessanterweise gibt es aus toxikologischer Sicht keinen greifbaren Grenzwert, ab welcher Konzentration eine krebserregende Substanz Krebs auslösen kann. Naja, auch als ich noch Alkohol getrunken habe, habe ich mir immer die Frage gestellt, wie das wäre, wenn Alkohol in der Gesellschaft so betrachtet werden würde wie andere, ähnlich schädliche Chemikalien. Der durchschnittliche Alkoholkonsum in Deutschland beträgt etwa 10,6 Liter pro Kopf, knapp 15% der Erwachsenen Menschen in Deutschland trinken so viel Alkohol, dass es gesundheitlich riskant ist.

Oder andersrum: Wie sollte über unbedenklichere Chemikalien nachgedacht werden, wenn gleichzeitig so viel Ethanol konsumiert wird? In der öffentlichen Wahrnehmung kommen Chemikalien sehr schlecht weg. Und es gibt Probleme mit Chemikalien. Das geht mir wieder an einem der letzten Tage am Strand durch denk Kopf: Mikroplastik. An jedem Strand der Welt befindet sich neben dem Sand auch Mikroplastik – winzige Kunststoffpartikel unter 5 Millimeter Größe. Die meisten Kunststoffe, und dazu gehören auch die Ausgangsstoffe für viele unserer alltäglichen Produkte wie PET-Flaschen, Dämmmaterial aus Polyurethan oder Wasserrohre aus PVC, sind chemisch sehr stabil und halten Jahre bis Jahrhunderte. Tolle und wichtige Eigenschaften, denn wenn ein PVC-Fenster lange hält und stabil gegen Witterung ist, muss es nicht mit anderen Chemikalien geschützt oder schnell ersetzt werden. Falsch verwendet und nicht richtig entsorgt gelangen Kunststoffe jedoch in die Umwelt. In den Sand, ins Meer, in die Nahrungskette und somit wieder zurück zu uns Menschen. Seit dem Jahr 2022 verhandeln aus diesem Grund die Vereinten Nationen ein Global Plastic Treaty, das Regeln zur weltweiten Kunststoffproduktion und Entsorgung schaffen soll.
Und hier schließt meine kleine Urlaubsgeschichte von Meer, von Sand, von Wasser und von der Chemie. Schreibt mir gerne, wo ihr Chemie in eurem Urlaub entdeckt habt.

Mit sandigen Grüßen
Hendrik Fischer